| Молярная масса вещества (Грамм/Моль) |
|
Формула химического вещества |
![Формула химического вещества]() |
Введение в химические формулы
Не секрет , что химические знаки позволяют изобразить состав сложного вещества в виде формул.
Химическая формула — это условная запись состава вещества посредством химических знаков и индексов.
Формулы различают молекулярные, структурные, электронные и другие.
Молекулярные формулы (H3P04, Fe203, А1(ОН)3, Na2S04, 02 и т.д.) показывают качественный (т.е. из каких элементов состоит вещество) и количественный (т.е. сколько атомов каждого элемента имеются в веществе) состав.
Структурные формулы показывают порядок соединения атомов в молекуле, соединяя атомы черточками (одна черточка — одна химическая связь между двумя атомами в молекуле).
Относительная атомная и молекуряная масса
Относительная атомная масса вещестав или элемента - это безразмерная величина. Почему безразмерная, ведь масса должна иметь размерность?
Причина в том что атомная масса вещества в кг очень мала и выражается порядком 10 в минус 27 степени. Что бы в расчетах не учитывать этот показатель, массу каждого элемента привели к отношению 1/12 массы изотопа углерода. По этой причине относительная атомная масса углерода и составляет 12 единиц.
Современные значения относительных атомных масс приведены в периодической системе элементов Д.И.Менделеева. Для большинства элементов указаны
среднеарифметические значения атомных масс природной смеси изотопов этих элементов.
Например, относительная масса водорода равна 1, а кислорода 16.
Относительная молекулярная масса простых и сложных веществ численно равна сумме относительных атомных масс атомов, входящих в состав молекулы.
Например, относительная молекулярная масса воды
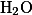
, состоящей из двух атомов водорода и одного атома кислорода, равна
1*2+16 =18
По химической формуле можно вычислить как химический состав, так и молекулярную массу.
Определяемый по химическим формулам количественный состав имеет огромное значение для многочисленных расчетов, которые производятся по химическому составу.
Вычисление относительной молекулярной массы вещества по химической формуле производится путем сложения произведений относительных атомных масс элементов на соответствующие индексы в химической формуле.
Как рассчитывается молекулярная масса вещества мы рассмотрели чуть выше.
И именно эту задачу автоматизирует наш химический калькулятор.
Зная молекулярную массу вещества, нам ничего не стоит рассчитать и молярную массу.
Моль - есть количество вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 12 грамм
Таким образом, молярная масса вещества с точностью соответствует относительной молекулярной массе и имеет размерность грамм/моль
Таким образом молярная масса воды равна 18 грамм/моль.
Молярную массу вещества можно определить как отношение массы данной порции вещества к количеству вещества в этой порции
Отличительные особенности
В отношении других калькуляторов, рассчитывающих молярную массу вещества, этот калькулятор обладает следующими особенностями:
- Формула может содержать скобки например 2*12H_2O}$)
- Формула может содержать коэффициент ![Na2[Zn(OH)4]](https://img.abakbot.ru/cgi-bin/mathtex.cgi?$\mathrm{Na_2[Zn(OH)4]}$)
Если есть необходимость рассчета массовых долей каждого химическго элемента в формуле то стоит воспользоваться калькулятором Массовая доля вещества онлайн
Интересные факты
Молярные массы каких химических элементов не округляются?
Логично, предположить если вы прочитали, откуда появляется понятие "относительная масса", что "не округленная" масса будет у одного элемента - углерода. Будут ли встречаться другие химические элементы с "не округленными" массами? Сомневаюсь.
синтаксис
molar формула[!]
где формула - произвольная формула химического вещества.
Внимание! Химические элементы в формуле должны быть указаны так, как в таблице Менделеева.
простой пример покажет какая цена ошибки не соблюдать регистр (прописные или строчные символы) букв
Если напишем CO - то это углерод и кислород, а если напишем Co - то это кобальт.
В любую часть формулы, можно вставить служебный символ(восклицательный знак).
Что же он нам дает?
Он все параметры огругляет до того уровня точности, который используется в школьной программе. Это очень удобно именно для тех, кто решает школьные задачи.
Например молярная масса воды 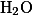 в школьных учебниках равна 18, а если учитывать более точные алгоритмы, то получаем что молярная масса равна 18.01528. Разница небольшая, но если делать расчет например массовой доли химического вещества, получается небольшое, но очень неприятное расхождение в выходных параметрах, которое может ввести в заблуждение неопытных пользователей калькулятора.
в школьных учебниках равна 18, а если учитывать более точные алгоритмы, то получаем что молярная масса равна 18.01528. Разница небольшая, но если делать расчет например массовой доли химического вещества, получается небольшое, но очень неприятное расхождение в выходных параметрах, которое может ввести в заблуждение неопытных пользователей калькулятора.
Примеры
Рассчитать молярную и молекулярную массу вещества 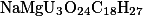
пишем запрос molar NaMgU3O24C18H27
получаем ответ
|
Молярная масса вещества (Грамм/Моль) |
|
1388.80945
|
|
Формула химического вещества |
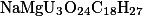 |
Если же в входных параметрах написать символ- восклицательный знак, то получим такой ответ
Молярная масса вещества равна 1389
Рассчитать молярную массу ![K_{4}[Fe(CN)6]](https://img.abakbot.ru/cgi-bin/mathtex.cgi?\mathrm{K_{4}[Fe(CN)6]})
Пишем K4[Fe(CN)6]
|
Молярная масса вещества (Грамм/Моль) |
|
368.3464
|
|
Формула химического вещества |
6]}$) |
Узнаем молекулярную, а также молярную массу 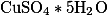
В результате запроc выглядит так molar CuSO4*5H2O
И ответ выглядит так
|
Молярная масса вещества (Грамм/Моль) |
|
249.68
|
|
Формула химического вещества |
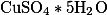 |
Как уже было сказано в статье выше, молярная масса и молекулярная масса вещества равны друг другу и отличаются лишь тем, что молекулярная масса безразмерная величина, в отличии от молярной массы (грамм/моль)
Удачных Вам расчетов!